от Автора: Christian Schneider, Max Planck Society
Давно известно, что люди могут вырабатывать защитные силы и, следовательно, антитела против вирусов. Но антитела могут вырабатываться и против полиэтиленгликоля (ПЭГ), вещества, используемого в косметике, продуктах питания и медицине. Это влияет на эффективность лекарств.
Группа исследователей из Института полимерных исследований Макса Планка в настоящее время исследовала, насколько широко эти антитела уже распространены в немецком обществе и как они могут повлиять на медикаментозную терапию с использованием наноносителей. Они опубликовали свои текущие результаты в журнале Nanoscale Horizons.
Вирус проникает в организм, и иммунная система начинает работать: вырабатываются антитела, которые борются с инфекцией. В то же время накапливается иммунная память, позволяющая быстро вырабатывать антитела в случае новой инфекции. Удивительно, но антитела могут также образовываться против полиэтиленгликоля (ПЭГ), молекулы с довольно простой структурой.
Помимо косметических средств — от кремов, духов и лосьонов до губной помады — полиэтиленгликоль также используется в медицине. Здесь он служит своего рода камуфляжной оболочкой против собственной иммунной системы организма, тем самым увеличивая время циркуляции активного ингредиента в крови.
«Для нас PEG интересен тем, что позволяет покрывать им наноразмерные носители лекарств», — говорит Свенья Морсбах, руководитель группы Катарины Ландфестер в отделе исследований полимеров MPI. Таким образом, исследователи добиваются более длительного времени циркуляции капсул с лекарством, размер которых составляет всего нанометры и которые, например, могут стать важным компонентом в новых методах лечения рака в будущем.
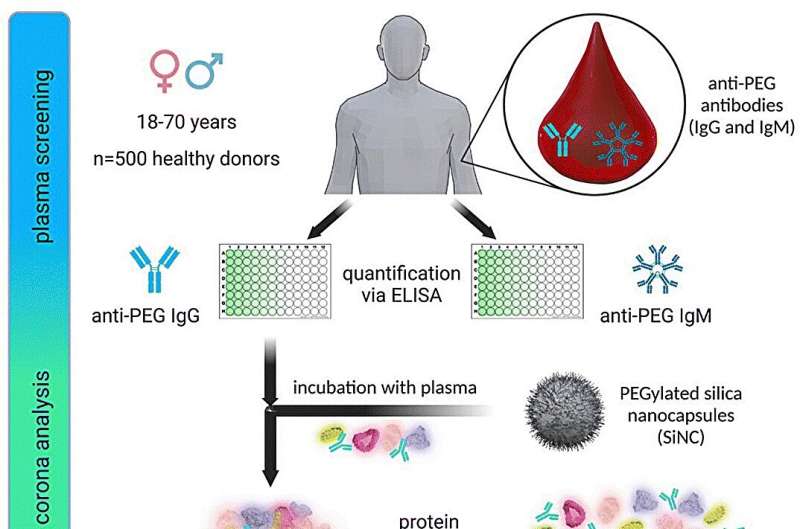
В своих исследованиях команда, возглавляемая Морсбахом и Ландфестером, изучила более 500 образцов крови пациентов, взятых в 2019 году. «Антитела, образующиеся против ПЭГ, прикрепляются к покрытым наноносителям, тем самым противодействуя желаемому эффекту: наноноситель становится видимым для иммунной системы и удаляется до того, как он сможет оказать свое действие», — объясняет Катарина Ландфестер, директор департамента.
Исследователи во главе с Морсбахом и Ландфестером предполагают, что в будущем методы лечения должны быть адаптированы к такому поведению иммунной системы. В ходе своих статистических исследований образцов крови они обнаружили, что антитела к ПЭГ уже были обнаружены в 83% исследованных образцов.
Концентрация ПЭГ-антител в крови непропорционально коррелирует с возрастом обследуемого: чем старше человек, тем меньше присутствовало ПЭГ-антител. «В настоящее время мы предполагаем, что это связано с растущим использованием ПЭГ в различных сферах жизни только в последнее время и изменением иммунной системы с возрастом», — говорит Морсбах.
В дальнейших исследованиях исследователи теперь хотели бы выяснить, как будущие методы лечения могут быть адаптированы, чтобы компенсировать уменьшенную маскировку наноносителей. «Идеи включали бы в себя вопрос о том, можно ли заменить PEG или, возможно, вообще обойтись без него», — сказал Морсбах. Но определение концентрации антител в крови пациента и индивидуальная корректировка количества активного ингредиента также могут быть альтернативой.
More information: Mareike F. S. Deuker et al, Anti-PEG antibodies enriched in the protein corona of PEGylated nanocarriers impact the cell uptake, Nanoscale Horizons (2023). DOI: 10.1039/D3NH00198A
Provided by Max Planck Society